
Máriatövis (Silybum marianum) – a máj védelmének tudománya
Máriatövis (Silybum marianum) – a máj védelmének tudománya: hagyomány, klinikai bizonyítékok és fitoterápiás szinergiák
Hogyan támogatja a máriatövis a májsejteket, mit bizonyított a modern orvostudomány, és miként működik együtt más gyógynövényekkel a májműködés optimalizálásában.
1. A máj – az emberi szervezet biokémiai központja, és miért vált a máriatövis a máj védelmének szimbólumává
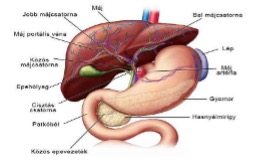
A máj az emberi szervezet egyik legösszetettebb és legnagyobb terhelésnek kitett szerve. Tömege felnőttkorban eléri az 1,3–1,6 kilogrammot, és több mint 500 ismert biokémiai folyamat zajlik benne folyamatosan, éjjel-nappal. Működése nem látványos, nincsenek idegvégződései, nem „fáj” addig, amíg a károsodás előre nem haladott – éppen ezért a máj egészsége sokáig láthatatlan marad.
A modern életmód azonban minden korábbinál nagyobb terhet ró erre a szervre. Feldolgozott élelmiszerek, alkohol, gyógyszerek, környezeti toxinok, endokrin diszruptorok, krónikus gyulladás, inzulinrezisztencia és tartós pszichés stressz együttesen alakítják ki azt a metabolikus környezetet, amelyben a máj már nem csupán alkalmazkodik, hanem kimerül.
Ebben az összefüggésben vált a májvédelem – hepatoprotekció – az elmúlt évtizedek egyik központi témájává a preventív orvoslásban és a tudományosan megalapozott fitoterápiában.
1.1 A máj valódi szerepe – túl a „méregtelenítés” mítoszán
A köznyelvben gyakran használt „méregtelenítés” kifejezés leegyszerűsíti a máj rendkívül kifinomult működését. Tudományos szempontból a máj nem tisztít, hanem biotranszformál. Ez a folyamat két fő szakaszra bontható:
- I. fázis – aktiváció: Oxidációs, redukciós és hidrolízises reakciók során a zsírban oldódó vegyületek (gyógyszerek, toxinok, hormonok bomlástermékei) reaktívabb köztes formává alakulnak. Ezek a köztes metabolitok gyakran reaktívabbak és potenciálisan károsabbak, mint az eredeti molekula.
- II. fázis – konjugáció: A szervezet ezeket a köztes termékeket vízoldékonnyá alakítja (glutation-, szulfát-, glükuronid- vagy aminosav-kötéssel), lehetővé téve az epével vagy a vesén keresztüli kiválasztást.
A máj egészsége tehát nem azon múlik, hogy „kimossuk-e”, hanem azon, hogy mennyire hatékonyak ezek az enzimatikus rendszerek, képesek-e kezelni az oxidatív stresszt, és mennyire védettek maguk a májsejtek (hepatociták) a krónikus gyulladással és toxikus terheléssel szemben.
1.2 A májsejt, mint sérülékeny, de regenerációra képes egység
A hepatociták különleges sejtek: extrém metabolikus aktivitással rendelkeznek és magas mitokondriumszámmal működnek, ugyanakkor rendkívül érzékenyek az oxidatív károsodásra. A máj egyik legnagyobb erénye a regenerációs képessége. Ez azonban nem korlátlan. Krónikus terhelés esetén:
- fokozódik a lipidfelhalmozódás (zsírmáj),
- aktiválódnak a gyulladásos útvonalak,
- megindulhat a kötőszövetes átépülés (fibrosis),
- végső esetben cirrhosis alakul ki.
1.3 A máriatövis megjelenése a májvédelem történetében

Ebbe a tudományos gondolkodásba illeszkedik bele a máriatövis, tudományos nevén Silybum marianum. Ez a mediterrán eredetű, lila virágú növény évszázadok óta kapcsolódik a májhoz – először empirikus megfigyelések, később egyre pontosabb kémiai és farmakológiai vizsgálatok alapján.
A máriatövis különlegessége nem abban rejlik, hogy „méregtelenít”, hanem abban, hogy:
- védelmet nyújt a májsejteknek a károsító hatásokkal szemben,
- támogatja a sejtek antioxidáns válaszát,
- és bizonyos körülmények között hozzájárulhat a májműködés biokémiai egyensúlyához.
1.4 Miért vált a máriatövis a „máj gyógynövényévé”?
A válasz nem egyetlen állításon alapul, hanem három tényező találkozásán:
- Hosszú történeti használat: A máriatövis a nyugati fitoterápia egyik legkonzisztensebb májhoz kötött növénye.
- Egyedülálló hatóanyag-komplex: A szilimarin flavonolignánjai olyan biológiai hatásokat mutatnak, amelyek közvetlenül illeszkednek a májsejtek védelmi mechanizmusaihoz.
- Kiterjedt tudományos vizsgálati háttér: Kevés gyógynövény rendelkezik olyan mennyiségű sejt-, állatkísérletes és humán klinikai adattal, mint a máriatövis.
1.5 Tudományos alapállás már az elején
Fontos ezt az esszét egyértelmű szakmai alapállással indítani: A máriatövis nem csodaszer. Nem helyettesíti az életmódváltást, az alkoholmegvonást vagy az orvosi kezelést. Nem „tisztítja ki” a májat egészséges emberekben. Ugyanakkor a rendelkezésre álló bizonyítékok alapján az egyik legjobban kutatott természetes hepatoprotektív növény, amely megfelelő kontextusban, reális elvárásokkal alkalmazva értékes része lehet egy komplex májtámogató stratégiának.
2. Botanika és történeti gyökerek – hogyan vált a máriatövis a máj gyógynövényévé?

A gyógynövények tudományos megértése mindig két, egymást kiegészítő pilléren nyugszik: a botanika pontosságán és a történeti használat kritikus értelmezésén. A máriatövis esetében ez a kettő különösen jól követhető ívet rajzol: egy mediterrán vadnövénytől egészen a modern hepatológiai kutatásokig.
2.1. Növénytani besorolás és morfológiai sajátosságok
A máriatövis tudományos neve Silybum marianum, a fészkesvirágzatúak (Asteraceae) családjába tartozó, egy- vagy kétéves növény.
Főbb botanikai jellemzők:
- 60–150 cm magasra növő, robusztus megjelenésű növény,
- nagy, fényes zöld levelek, jellegzetes fehér márványozott erezettel,
- bíbor-lila virágzat,
- termése kaszattermés, amely a hatóanyagok szempontjából döntő jelentőségű.
A májvédő hatás nem a levélhez vagy a virághoz, hanem szinte kizárólag a maghoz (terméshez) kötődik. Ez kulcsfontosságú szakmai megkülönböztetés, mivel a nem megfelelő növényi rész felhasználása jelentősen csökkentheti a biológiai hatást.
2.2. Földrajzi eredet és elterjedés
A máriatövis eredeti elterjedési területe a mediterrán térség (Dél-Európa, Észak-Afrika, Közel-Kelet nyugati régiói). A növény kiválóan alkalmazkodik: száraz, napos területekhez, gyengébb minőségű talajhoz, ember által bolygatott környezethez. Ez az ökológiai rugalmasság tette lehetővé, hogy a máriatövis már az ókorban széles körben elérhető legyen, és hamar bekerüljön a helyi gyógyászati gyakorlatba.
2.3 – 2.4 Történeti áttekintés
A máriatövis legkorábbi írásos említései az antik görög–római orvoslásból származnak. Bár ekkor még nem ismerték sem a máj biokémiai szerepét, sem a hatóanyagokat, a növény empirikus alkalmazása már ekkor emésztéssel, epével és „belső tisztulással” kapcsolódott össze. A középkorban a máriatövis már stabil helyet foglalt el az európai gyógynövényes könyvekben: a májat a „test nedveinek” központjaként tartották számon.
2.5. A fordulópont: fitokémia és modern farmakológia
A máriatövis történetében a valódi tudományos fordulópont a 20. század közepén következett be, amikor izolálták a mag fő hatóanyag-komplexét, azonosították a flavonolignánokat, és elkezdődtek az első kontrollált farmakológiai vizsgálatok. Ettől a ponttól kezdve a máriatövis kilépett a pusztán tradicionális gyógynövény szerepből, és a modern hepatoprotektív kutatások egyik modellnövényévé vált.
3. Hatóanyag-profil – mi is valójában a szilimarin, és miért kulcskérdés a minőség?
A máriatövis májvédő hatása nem általános „növényi kivonat” jellegű tulajdonság, hanem egy jól körülhatárolható, kémiailag definiált hatóanyag-együtteshez kötődik. A hatás szempontjából meghatározó növény a Silybum marianum termése (kaszattermése), azon belül is egy komplex fitokémiai frakció: a szilimarin.
A „szilimarin” elnevezés félrevezető lehet, mert nem egyetlen molekulát, hanem flavonolignánok keverékét jelenti. Fő komponensei: szilibinin (silybin A és B – a biológiailag legaktívabb frakció), szilikrisztin, szilidianin, izoszilibinin.
A máriatövis hatóanyagai szinte kizárólag a termésben koncentrálódnak. A modern fitoterápiában a standardizálás nem marketingfogalom, hanem tudományos minimumfeltétel. A máriatövis esetében ez jellemzően 70–80% szilimarin-tartalomra standardizált kivonatot jelent, meghatározott szilibinin-aránnyal.
3.4. Biohasznosulás – a máriatövis Achilles-sarka
A szilimarin egyik legnagyobb kihívása a rossz vízoldékonyság és alacsony felszívódás. Klasszikus kivonatok esetében az orális biohasznosulás alacsony, a plazmakoncentráció gyorsan csökken. Ez a tény hosszú ideig megkérdőjelezte a klinikai hatásosságot, amíg meg nem jelentek a komplexált (pl. foszfolipidhez kötött) formulák és biohasznosulást javító technológiák.
4. Hatásmechanizmusok – hogyan védi a szilimarin a májsejteket sejtszinten és molekuláris szinten?

A máriatövis tudományos megítélésének kulcsa nem az, hogy „jó-e a májnak”, hanem az, hogy milyen biológiai útvonalakon keresztül fejti ki hatását, és ezek az útvonalak összhangban állnak-e a májkárosodás modern patofiziológiai modelljeivel.
4.1. Oxidatív stressz csökkentése – a Nrf2–ARE tengely aktiválása
A krónikus májkárosodás egyik központi mozgatórugója az oxidatív stressz. A szilimarin egyik legjobban dokumentált hatása, hogy nem egyszerűen antioxidáns módon „semlegesíti” a szabad gyököket, hanem aktiválja a sejtek saját antioxidáns védelmi rendszerét (Nrf2 útvonal).
4.2. Gyulladáscsökkentő hatás – NF-κB és MAPK jelátviteli utak modulálása
A májkárosodás nem pusztán oxidatív, hanem gyulladásos folyamat is. A szilimarin csökkenti az NF-κB aktivációját és mérsékli a gyulladásos citokinek termelődését.
4.3. Hepatocita-membrán stabilizálás és toxinvédelem
A májsejtek membránja az egyik elsődleges célpontja alkoholnak, gyógyszermetabolitoknak és toxinoknak. A szilimarin egyik klasszikus hatása, hogy stabilizálja a hepatocita-membránt, csökkenti bizonyos toxikus vegyületek sejtbe jutását, és mérsékli a lipidperoxidációt.
4.4. Antifibrotikus hatások
A krónikus májbetegségek egyik legkritikusabb pontja a fibrosis (kötőszövetes átépülés). Preklinikai vizsgálatokban a szilimarin gátolta a máj csillagsejtjeinek aktivációját, bár humán klinikai vizsgálatokban a fibrosis regressziója nem egyértelműen bizonyított.
4.5. Mitokondriális védelem és sejtszintű energiaegyensúly
Újabban egyre több adat utal arra, hogy a szilimarin javíthatja a mitokondriális funkciót és csökkentheti a mitokondriális ROS-termelést, ami különösen releváns zsírmáj és inzulinrezisztencia esetén.
Összegzés: A szilimarin hatásmechanizmusai nem egyetlen „csodahatásra” épülnek, hanem több, egymást erősítő biológiai útvonal finomhangolására: endogén antioxidáns védelem erősítése, krónikus gyulladás mérséklése, hepatocita-membrán stabilizálása.
5. Klinikai vizsgálatok – mit igazolnak az emberi adatok, és hol vannak a bizonyítékok határai?
A máriatövis körüli szakmai viták nem azért vannak, mert „nincs róla kutatás”, hanem mert sokféle készítményt, dózist, betegcsoportot és végpontot vizsgáltak.
5.1. Zsírmáj (NAFLD / MAFLD) és NASH
Ez a legtöbbet vizsgált terület. A metaanalízisek szerint a szilimarin-alapú terápiák esetén gyakran javulnak a májenzimek (ALT/AST), és néha javulnak a metabolikus paraméterek is. A „szilibin fitoszóma + E-vitamin” modell különösen erős klinikai jeleket mutatott (májenzimek, inzulinrezisztencia javulása). Ugyanakkor a biopsziás fibrosis-végpontok tekintetében az eredmények még vegyesek.
5.2. Alkoholos májbetegség és cirrhosis
Bár történelmileg ez a legismertebb terület, az eredmények ellentmondásosak. Egyes vizsgálatok túlélési előnyt valószínűsítettek, mások nem találtak egyértelmű bizonyítékot a mortalitás csökkenésére. Cirrhosisban a szilimarin legfeljebb kiegészítő, májsejt-védelmi jellegű eszköz lehet.
5.3. Vírushepatitis (HBV / HCV)
Nem áll rendelkezésre meggyőző bizonyíték arra, hogy a máriatövis csökkentené a vírusmennyiséget vagy kiváltaná az antivirális kezelést. Támogató jelleggel, orvosi kontroll mellett értelmezhető.
5.4. Mérgezések (Gyilkos galóca)
Az intravénás szilibinin a patomechanizmushoz illeszkedve releváns lehet, de a magas minőségű randomizált bizonyítékok érthető okokból (ritka, életveszélyes állapot) korlátozottak.
Amit a tudomány támogat: NAFLD/MAFLD esetén a májenzimek és metabolikus állapot javítása. Amit nem szabad ígérni: „Méregtelenítés”, vírushepatitis gyógyítása, cirrhosis biztos visszafordítása.
6. Fitoterápiás szinergiák a máj támogatásában – miért rendszer a máj, és miért rendszer a fitoterápia?
A máj nem egyetlen funkciót lát el, hanem egy komplex biológiai hálózat központja. A tudományosan megalapozott fitoterápia ezért nem izolált hatásokban, hanem szinergikus rendszerekben gondolkodik. Ebben a rendszerben a máriatövis központi szerepet tölt be, de nem önmagában, hanem olyan növényekkel együtt, amelyek a máj működésének különböző tengelyeit támogatják.
6.1. Hepatocita-védelem és oxidatív stressz – a máriatövis mint központi elem
A máriatövis szilimarin-komplexe a májtámogató rendszer stabilizáló magja. Aktiválja az endogén antioxidáns válaszokat és védi a hepatociták integritását. Ez az alap, amely nélkül a többi növény hatása kevésbé lenne értelmezhető.
6.2. Antioxidáns háttér és gyulladáscsökkentés
A hepatocita-védelem akkor válik teljessé, ha külső antioxidáns és gyulladáscsökkentő háttér is társul. Ebben játszik szerepet például a Capparis spinosa (kapribogyó), amely funkcionálisan kiegészíti a máriatövis hatását.
6.3. Metabolikus–máj tengely – amikor a zsírmáj nem csak „májkérdés”

A modern májterhelés egyik leggyakoribb formája a metabolikus eredetű zsírmáj. Itt a probléma nem elsősorban toxikus, hanem anyagcsere-eredetű. Ebben a kontextusban az Articsóka (Cynara scolymus) kulcsszereplő: fokozza az epeelválasztást és támogatja a lipidanyagcserét. Ehhez társul a Mezei katáng (Cichorium intybus), amely befolyásolja a glükóz- és lipidanyagcserét. Ebben a hármasban (máriatövis, articsóka, katáng) a máj kevesebb terhelést kap, miközben védettebbé válik.
6.4. Epeáramlás és kiválasztás – a „detox” valós biológiája
A máj által végzett biotranszformáció csak akkor válik teljessé, ha a kiválasztás is megfelelően működik. Ebben a tengelyben a cickafark (Achillea millefolium) és a Tamarix gallica szerepe indokolt: koleretikus hatás, emésztési komfort javítása, epeeredetű panaszok enyhítése. Ez teszi lehetővé, hogy a „méregtelenítés” fogalmát tudományosan korrekt módon használjuk: nem tisztításról, hanem a kiválasztási kapacitás támogatásáról beszélünk.
6.5. Adaptogén és ayurvédikus kiegészítés
A krónikus májterhelés gyakran adaptációs kudarc. Ebben a folyamatban kap szerepet több ayurvédikus növény (Terminalia bellirica, Terminalia arjuna, Phyllanthus emblica), amelyek antioxidáns és adaptogén hatásukkal segítik a krónikus terheléshez való alkalmazkodást.
6.6. Gyulladás moduláció – az édesgyökér szerepe
A Glycyrrhiza glabra (édesgyökér) gyulladáscsökkentő hatása miatt értékes precízen adagolt modulátor lehet a rendszerben.
Összefoglaló
A máriatövis (Silybum marianum) hatóanyag-komplexe, a szilimarin a modern fitoterápia egyik legjobban kutatott hepatocita-védő természetes összetevője. Tudományosan igazolt hatásai elsősorban a májsejtek oxidatív stresszel és gyulladásos károsodással szembeni védelméhez, a sejtmembrán stabilizálásához, valamint az endogén antioxidáns rendszerek aktiválásához kapcsolódnak.
A modern májterhelés indokolja a szinergikus fitoterápiás megközelítést, amelyben a szilimarin központi, de nem kizárólagos szerepet tölt be. Más gyógynövényekkel (pl. articsóka, katáng, cickafark) kombinálva a hatás kiterjeszthető az epe- és lipidanyagcserére, valamint a metabolikus folyamatok támogatására. A máriatövis nem csodaszer, hanem egy tudományosan jól értelmezhető, központi hepatoprotektív elem.
Irodalomjegyzék
- Friedman, S.L., Neuschwander-Tetri, B.A., Rinella, M. & Sanyal, A.J. (2018) Mechanisms of NAFLD development and therapeutic strategies. Nature Medicine, 24(7), pp. 908–922.
- Tilg, H., Adolph, T.E., Moschen, A.R. (2021) Multiple parallel hits hypothesis in NAFLD revisited. Hepatology, 73(2), pp. 833–842.
- Abenavoli, L., Capasso, R., Milic, N. & Capasso, F. (2010) Milk thistle in liver diseases: past, present, future. Phytotherapy Research, 24(10), pp. 1423–1432.
- Federico, A. et al. (2017) Silymarin in non-alcoholic fatty liver disease: A systematic review. World Journal of Hepatology, 9(22), pp. 973–985.
- Polyak, S.J. et al. (2013) Silymarin for HCV infection. Hepatology, 57(3), pp. 1260–1267.
- Saller, R. et al. (2008) An updated systematic review of the pharmacology of silymarin. Drugs, 68(6), pp. 821–840.
- Loguercio, C. et al. (2012) Silybin combined with phosphatidylcholine and vitamin E in patients with nonalcoholic fatty liver disease: A randomized controlled trial. Free Radical Biology and Medicine, 52(9), pp. 1658–1665.
- Loguercio, C. & Festi, D. (2011) Silybin and the liver: from basic research to clinical practice. World Journal of Gastroenterology, 17(18), pp. 2288–2301.
- Panahi, Y. et al. (2018) Efficacy of artichoke leaf extract in non-alcoholic fatty liver disease: A randomized controlled trial. Phytotherapy Research, 32(7), pp. 1382–1387.
- Wider, B. et al. (2009) Artichoke leaf extract for treating hypercholesterolaemia. Phytomedicine, 16(8), pp. 718–724.
- Zafar, R. & Mujahid Ali, S. (1998) Anti-hepatotoxic effects of roots and root callus extracts of Cichorium intybus. Journal of Ethnopharmacology, 63(3), pp. 227–231.
- EMA (2013) Assessment report on Cichorium intybus L., radix. European Medicines Agency.
- Ebrahimi-Mameghani, M. et al. (2022) Effects of Achillea millefolium supplementation on liver enzymes and metabolic parameters in patients with type 2 diabetes: A randomized controlled trial. Journal of Herbal Medicine, 31, 100519.
- EMA (2014) Assessment report on Achillea millefolium L., herba. European Medicines Agency.
- Jalali, M.T. et al. (2019) The effects of licorice extract supplementation on NAFLD: A randomized controlled clinical trial. Phytotherapy Research, 33(7), pp. 1993–2001.
- Isbrucker, R.A. & Burdock, G.A. (2006) Risk and safety assessment on the consumption of licorice root. Regulatory Toxicology and Pharmacology, 46(3), pp. 167–192.
- Dwivedi, S. (2007) Terminalia arjuna Wight & Arn.—A useful drug for cardiovascular disorders. Journal of Ethnopharmacology, 114(2), pp. 114–129.
- Kumar, S. et al. (2010) Hepatoprotective activity of Terminalia arjuna bark extract. Journal of Ethnopharmacology, 127(3), pp. 609–615.
- Baliga, M.S. & Dsouza, J.J. (2011) Amla (Emblica officinalis Gaertn), a wonder berry in the treatment and prevention of cancer. European Journal of Cancer Prevention, 20(3), pp. 225–239.
- Krishnaveni, M. & Mirunalini, S. (2010) Therapeutic potential of Phyllanthus emblica in liver disorders. Journal of Basic and Clinical Physiology and Pharmacology, 21(3), pp. 1–14.
- Ben Saad, A. et al. (2014) Hepatoprotective and antioxidant effects of Tamarix gallica extracts. Biomedicine & Preventive Nutrition, 4(3), pp. 329–336.
- Ksouri, R. et al. (2009) Medicinal properties of Tamarix species. Journal of Medicinal Plants Research, 3(7), pp. 399–405.
- Cochrane Hepato-Biliary Group (2017) Milk thistle for chronic liver diseases. Cochrane Database of Systematic Reviews, CD003620.
- EASL (2021) Clinical Practice Guidelines on non-alcoholic fatty liver disease. Journal of Hepatology, 75(4), pp. 833–883.

